Primum non nocere: la necesidad de reemplazar la experimentación animal en la investigación de enfermedades neurodegenerativas
19/04/2024
19/04/2024
Por:
Luis Falcón
Luis Falcón, MD, MSc
Científico Computacional
Médico
Master en Genómica y Genética Médica
Presidente de ONG GNU Solidario
Autor de GNU Health
Director Médico del Centro de Medicina de Precisión y Salud Integrativa – PrecisionMed –
Las enfermedades neurodegenerativas comprenden un amplio espectro de patologías que afectan al sistema nervioso. Son procesos crónicos y progresivos que generan un gran impacto físico, emocional, social y económico en el paciente y sus familiares.
Estudios epidemiológicos muestran un alza en la incidencia y prevalencia de enfermedades neurodegenerativas a nivel global, lo que representa un reto fenomenal desde el punto vista de la Salud Pública, en una sociedad cada vez más longeva.
La investigación biomédica en procesos neurodegenerativos y demencia ha tenido pocos resultados, con un índice de fracaso superior al 99%. La mayoría de los fármacos no sólo no consiguen revertir la evolución de la enfermedad, sino que generan efectos adversos y un elevado coste económico.
Como sociedad y como comunidad científica estamos obligados a reflexionar sobre el modelo actual de investigación biomédica. Un modelo anacrónico y cruel, ligado íntimamente al uso de experimentación animal, que no sólo supone un problema ético irrefutable, sino que ha resultado ser un fracaso en términos prácticos y que nos exige un cambio radical de paradigma.
Es este artículo se resumen los avances en alternativas éticas a la experimentación animal que relevantes a la fisiología humana, tales como estudios in vitro (organ-on-a-chip) o in silico (modelos computacionales) e investigación del exposoma, que arrojan luz sobre la investigación biomédica en las enfermedades neurodegenerativas y la demencia.
La prevalencia e incidencia de las enfermedades neurodegenerativas sigue al alza. Actualmente más de 9.8 millones de individuos sufren demencia en Europa. Se espera que para el año 2050 la cifra se duplique, superando 18.8 millones [1]. Esto equivaldría aproximadamente a la suma de la población actual de Grecia y Portugal.
La Organización Mundial de la Salud reporta 66 millones de personas que padecen demencia en el mundo [2]. Se estima que para el 2050, el número de personas que padezcan demencia superará los 150 millones [3]
Las enfermedades neurodegenerativas con mayor prevalencia son la enfermedad de Alzheimer (AD) y la enfermedad de Parkinson (PD). En cuanto a las principales causas de demencia, la enfermedad de Alzheimer (AD) y la demencia vascular ocupan el primer y segundo puesto respectivamente.
Además de la tremenda carga física, emocional y social para el paciente y su familia, las enfermedades neurodegenerativas suponen un altísimo coste económico al sistema de salud. Se estima que el coste medio por paciente que sufre demencia es de € 22.000 al año. A nivel Europa, la cifra asciende a € 177 billones [4].
Las enfermedades neurodegenerativas son procesos elusivos, crónicos y progresivos. La mayoría son multifactoriales, donde coexisten e interactúan factores genéticos y determinantes ambientales. Como en la mayoría de los casos de enfermedades multifactoriales, elucidar el agente etiológico sigue siendo un reto.
La enfermedad puede debutar después de años de evolución subclínica, de manera insidiosa y poco específica (cambios en el estado de ánimo, lagunas de memoria, trastorno del sueño…). Con el paso del tiempo, el número y severidad de las manifestaciones clínicas aumenta. Lamentablemente, muchos procesos neurodegenerativos terminan en demencia.
Los estadíos avanzados de muchas enfermedades neurodegenerativas comparten características desde el punto de vista clínico, anatómico y radiológico. Déficit de distintos dominios cognitivos, disminución de población neuronal, involución de masa cerebral, atrofia cortical, surcos y ventrículos cerebrales mucho más prominentes para la edad del individuo.
En la siguiente figura se compara una resonancia magnética fisiológica (a) [5] con las características radiológicas comunes en pacientes que sufren distintos tipos de demencia: Alzheimer (b) [6], demencia por cuerpos de Lewy (c) [7] y demencia vascular (e) [8]. En muchas ocasiones, los signos radiológicos se solapan, haciendo aún más complejo el diagnóstico. En este ejemplo, en la resonancia magnética del paciente con enfermedad de Alzheimer también se observan hiperintensidades periventriculares típicas de enfermedad vascular.
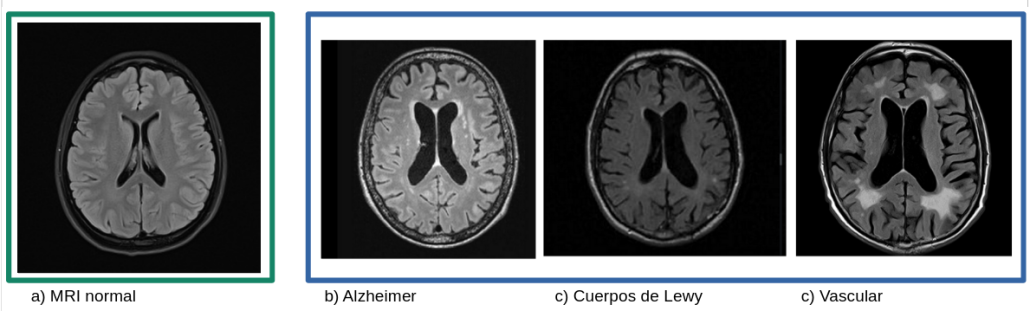
Comparativa de hallazgos radiológicos en demencias de distinto origen» Fuentes 5, 6, 7, 8
Podría resumirse el fracaso de la experimentación animal en la investigación biomédica con la frase del Dr. Thomas Hartung “los humanos definitivamente no son ratones de 70kg” [9]. Los humanos tenemos una anatomía, genética y fisiología única, que requieren una investigación biomédica con métodos relevantes a la fisiología humana.
En la mayoría de los casos, ensayos “prometedores” en la fase pre-clínica (experimentación animal) fracasan en la traslación a la fase clínica (en humanos). De hecho, el 96% de los experimentos con animales son un fracaso. [10]
En el caso concreto de la investigación relacionada con enfermedades neurodegenerativas, la tasa de fracaso es del 99.6% [11]. Esto nos debe hacer reflexionar y aplicar el dicho “si algo no funciona, debe cambiarse”. Más allá de las razones éticas, una tasa de acierto inferior al 1% tiene mucho de fuerza bruta y muy poco de científico. Resulta alarmante que al día de hoy se permita y perpetúe este fracaso y el coste de millones de vidas.
Avances en la informática médica, dispositivos como Organ-on-a-Chip, organoides y modelos computacionales nos brindan excelentes alternativas a la experimentación animal, relevantes a la fisiopatología humana.
Antes de detallar los métodos tecnológicos, debemos fijar los fundamentos éticos para la investigación biomédica, que también serán la base para el avance de nuestra sociedad.
Una ciencia que lastima, no es ciencia. Cada año más 115 millones de animales son usados en la experimentación animal [12]. secuestrados, enjaulados, sometidos a crueles experimentos y finalmente se les mata. Algunos utilizan el eufemismo “eutanasia”.
Recordamos las atrocidades realizadas en nombre de la ciencia por Mengele en niños gitanos o judíos. Atrocidades similares se realizan a diario en universidades y centros de investigación, siendo las víctimas primates no humanos, perros, gatos, cerdos o ratones. Estos animales son personas con capacidad de sufrir. La Declaración de Toulon recoge que los animales deben considerarse universalmente como personas y no como cosas. Desde la perspectiva del derecho, la situación jurídica de los animales cambiará en la medida en que se los eleve al rango de sujetos de derecho. [13]
Mengele realizaba los terribles experimentos en niños gemelos porque los despersonalizaba, deshumanizaba y cosificaba. La discriminación, en este caso basada en el grupo étnico, lo situaba en una posición moral superior, legitimizando los crueles experimentos, más aún cuando el fin era el avance de la medicina.
De la misma manera que detestamos los experimentos con humanos, no podemos romantizar la figura del científico con bata blanca que sostiene a un ratón por la cola. Cualquier tipo de discriminación, sea sexismo, racismo o especismo es detestable y debe ser erradicada de nuestra sociedad (para saber más pincha AQUI).
La máxima “primum non nocere” (lo primero, no hacer daño) que aplicamos en nuestro día a día con nuestros pacientes no puede ser limitada al ser humano. Como profesionales de la salud y como miembros de la comunidad científica debemos ser un ejemplo para la sociedad de benevolencia, compasión y empatía hacia el prójimo y de manera universal, independientemente de la especie.
Una vez erradicada la posibilidad de experimentar con animales no humanos, se abre un abanico de alternativas éticas y relevantes a la fisiología humana.
Salvo excepciones de origen netamente genético (ej, enfermedad de Huntington, early-onset Alzheimer), las enfermedades neurodegenerativas son multifactoriales, generadas por la interacción de factores genéticos y ambientales.
Gary Miller y Dean Jones definen el exposoma como “La medida acumulativa de las influencias ambientales y las respuestas biológicas asociadas a lo largo de la vida, incluidas las exposiciones del medio ambiente, la dieta, el estilo de vida y los procesos endógenos” [14]
La exposición a noxas ambientales o un estilo de vida poco saludable están asociados procesos epigenéticos que alteran la expresión génica, así como a la promoción de una cascada de eventos inflamatorios, aumentando el riesgo de patologías de carácter inmune, inflamación crónica de bajo grado (low-grade chronic inflammation), cáncer o enfermedades neurodegenerativas, entre otras.
En la investigación de las enfermedades neurodegenerativas, tan importante es el estudio de las bases moleculares de la enfermedad como la investigación de los determinantes ambientales y socioeconómicos de la misma. El ignorar los factores ambientales es quedarnos anclados en lo que denomino el “sistema de la enfermedad”, que únicamente reacciona a un proceso patológico ya presente, en vez de prevenir la aparición del mismo.
Estudios sugieren que el 33% de los casos de Alzheimer son consecuencia de los siguientes siete factores de riesgo: diabetes, hipertensión arterial -principalmente en mediana edad-, obesidad, tabaquismo, depresión, falta de estimulación cognitiva y bajo nivel académico [15] . La exposición a agentes ambientales como el humo del tráfico, monóxido de nitrógeno (NO) y monóxido de carbono (CO) y la exposición a micropartículas (PM) incrementan el riesgo de la enfermedad de Alzheimer (AD) y demencia [16] .
El proyecto del Exposoma Global (Global Exposome Project) [17] de GNU Solidario tiene el objetivo de investigar y difundir el rol del exposoma en el humano y otras especies, así como el impacto que tiene el ser humano como agente etiológico de enfermedades medioambientales. Los proyectos que participan del Exposoma Global no utilizan modelos animales, son publicados bajo licencia abierta (ej. Creative Commons) y usan Software Libre.
Stiletto [18], parte del proyecto del Exposoma Global, tiene como objetivo generar un modelo de la microcirculación cerebral en situaciones fisiológicas y patológicas. El proyecto estudiará las arterias perforantes y su relación con la unidad neurovascular (NVU). También investigará las bases moleculares y determinantes ambientales en angiopatías con base genética (CADASIL) y adquiridas (Binswanger) propias de estos vasos, ya que la enfermedad de pequeño vaso es la causa principal de deterioro cognitivo de origen vascular [19].
Las arterias perforantes lenticuloestriadas son pequeños vasos ( ⌀ 469 µm medio) [20] que se originan de la arteria cerebral media y nutren áreas cerebrales profundas como los ganglios basales. Las variantes anatómicas, recorrido e histología de dichos vasos son específicas del humano y exige estudiarlas en modelos relevantes a la anatomía, fisiología y genética humana.
Stiletto investigará el exposoma de los distintos grupos poblacionales que formen parte del estudio, y su posible relación con factores ambientales y epigenéticos asociados al inicio, severidad y progresión de las patologías. También pretende estudiar la edad como factor independiente en el desarrollo y evolución de la enfermedad.
Organ-on-a-chip (OoC) y organoides suponen uno de las mayores y prometedoras tecnologías que pueden ser aplicadas en múltiples escenarios de la investigación biomédica. Desde enfermedades metabólicas o inflamatorias a cáncer.
Organ-on-a-Chip permite cultivar células humanas en ambientes controlados. Desde células pluripotenciales inducidas (iPS) a células tumorales extraídas del propio paciente. Esta tecnología permite recrear, in vitro, condiciones fisiológicas y patológicas en distintos tejidos y órganos. De ahí los términos lung-on-a-chip, liver-on-a-chip, kidney-on-a-chip o, en nuestro caso, brain-on-a-chip.
La tecnología de organ-on-a-chip también brinda una plataforma extraordinaria para el estudio y desarrollo de nuevas drogas. Como muestra el siguiente diagrama, la tecnología organ-on-a-chip puede ser usada de manera individual o integrada a otros componentes de la Métodologías de nuevo enfoque (New Approach Methodologies – NAM -) [21]para estudios toxicológicos y desarrollo de nuevas drogas.
Como resultado se desarrollarán medicamentos más específicos, más seguros, con menos efectos secundarios y más eficaces.
Brain-on-a-chip
La barrera hematoencefálica (BBB) y la unidad neurovascular (NVU) son dos componentes clave en el estudio del sistema nervioso central y de enfermedades neurodegenerativas. Los procesos neurodegenerativos están íntimamente asociados a la disfunción de la unidad neurovascular. Tanto la barrera hematoencefálica como la unidad neurovascular son estructuras complejas que involucran procesos más complejos aún, que deben estudiarse en el contexto de la anatomía, histología, fisiología y genética de la especie humana.
Como ejemplo notable de las metodologías de nuevo enfoque quiero citar el trabajo de Ahn, Y., et al, quienes han conseguido generar organoides de vasos sanguíneos (Blood vessel organoids – BVO) que a su vez penetran organoides del parénquima cerebral [22]. Este experimento es fascinante, porque no sólo han conseguido cultivar y diferenciar células y tejidos específicos de órganos humanos, reprogramando células madres pluripotenciales de médula ósea humana (Human Induced Pluripotent Stem Cells -hiPSCs-) sino que se han conseguido la interacción entre ambos organoides.
En el contexto de enfermedades neurovasculares, nos brinda los elementos relevantes a la neurofisiología humana donde poder investigar la fisiopatología de distintos procesos degenerativos y el desarrollo de nuevos fármacos mucho más eficaces y seguros.
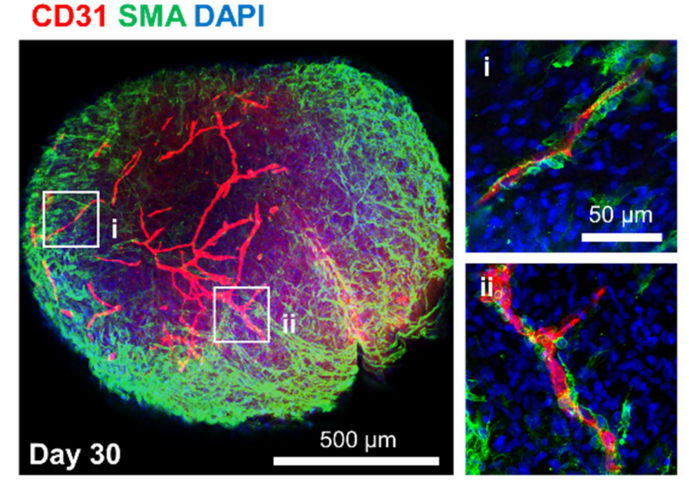
Identificación de estructuras tipo vaso sanguíneo incl. redes endoteliales y músculo liso en un organoide cerebral vascularizado. Crédito: Human Blood Vessel Organoids Penetrate Human Cerebral Organoids and Form a Vessel-Like System. https://doi.org/10.3390/cells10082036 (CC-by-SA)
No es ciencia ficción. Es una realidad y representa lo que debe ser el presente y futuro de la investigación biomédica.
Una de las características que comparten las enfermedades neurodegenerativas es que, en general, los signos aparecen a partir de la mediana edad y la prevalencia aumenta exponencialmente a partir de la séptima y octava década de vida.
En condiciones de laboratorio tradicionales, es imposible reproducir los complejos procesos relacionados con el envejecimiento y senescencia celular, más aún cuando están asociados a una enfermedad neurodegenerativa. La experimentación animal no puede reproducir estos procesos, por muchos motivos. Por ejemplo, la esperanza de vida de un ratón no suele superar los dos años, un periodo 40 veces menor al del humano.
Lo que si puede reproducir de manera mucho más fidedigna son modelos computacionales, tomando como base el conocimiento de la fisiología y anatomía humana. Los modelos computacionales pueden recrear infinidad de escenarios, viajar en el tiempo, introducir factores ambientales, variaciones anatómicas, agregar patologías co-existentes, evaluar el efecto de una droga, aprender de experimentos anteriores… Tecnología moderna para una medicina de precisión.
Ciencia abierta y redes federadas en la investigación biomédica
La ciencia no debe desarrollarse en silos ni que el acceso a la literatura científica sea privilegio de unos pocos. La ciencia no debe ser movida por la competencia ni por fines económicos. El desarrollo científico debe basarse en la cooperación, colaboración y la búsqueda genuina del desarrollo de nuestras sociedades.
Debemos abrazar la ciencia abierta. La ciencia abierta permite el acceso universal que exponencia el conocimiento y la investigación. El acceso a base de datos federadas globales con información sobre los factores ambientales, determinantes socioeconómicos y bases moleculares de la enfermedad, dará luz al rol del exposoma y a la correlación genotipo – fenotipo en enfermedades multifactoriales, tan devastadoras como elusivas, como el cáncer, patologías autoinmunes y procesos neurodegerativos. En definitiva, la ciencia abierta potenciará la investigación y acelerará los métodos de diagnóstico y tratamiento de muchas enfermedades y de los millones de personas que las padecen.
En el caso de GNU Health [23], el ecosistema de salud digital de software libre, podemos generar redes federadas de salud a nivel regional o global donde instituciones de investigación, profesionales de salud e individuos pueden actualizar la información de los distintos dominios de la salud.
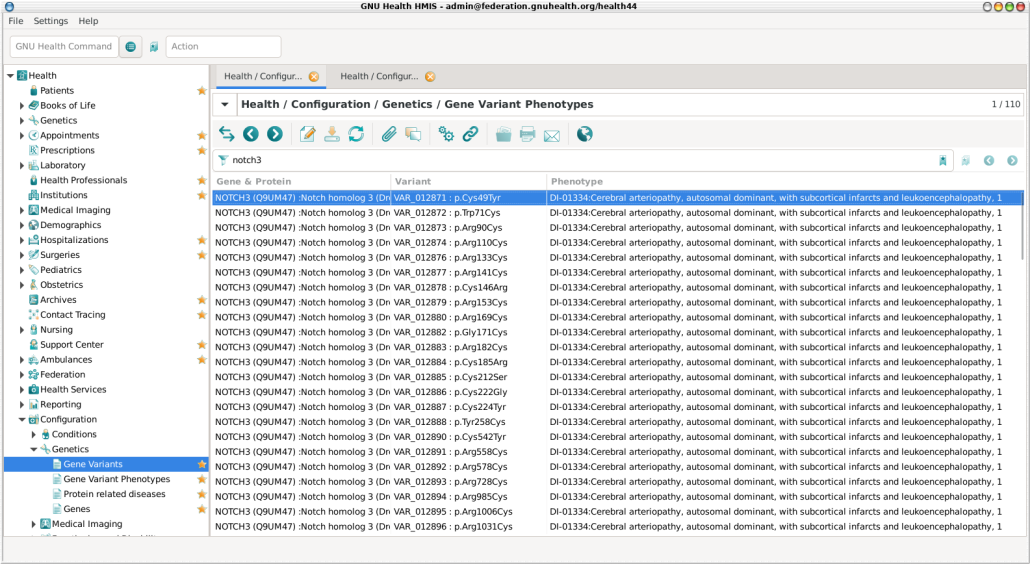
El sistema de Gestión Hospitalaria GNU Health mostrando las variantes naturales de Uniprot asociadas al gen NOTCH3 y con la enfermedad de pequeño vaso CADASIL
A su vez, GNU Health utiliza la base de datos de variantes naturales de Uniprot [24], generando una retroalimentación positiva de colaboración comunitaria, base de la ciencia abierta.
En resumen, la investigación biomédica debe evolucionar desde la compasión y el profundo respeto hacia todos los seres con los que compartimos este mundo, independientemente de la especie. El 99% de índice de fracaso de la experimentación animal en el contexto de enfermedades neurodegenerativas nos exige un cambio inmediato -en lo ético y en lo práctico- si realmente queremos encontrar una solución para los millones de personas que actualmente padecen Alzheimer, Parkinson, enfermedad neurovascular u otro proceso neurodegenerativo. Reducir la incidencia y prevalencia de la demencia en nuestra sociedad también está en manos de los gobiernos, que deben inviertir en ciencia abierta, aplicar políticas de salud pública contra la polución medioambiental, los determinantes socioeconómicos de la enfermedad así como aumentar la inversión en educación y estilos de vida saludables.
Es hora de un cambio radical de paradigma, donde se erradique el cruel, anacrónico y fallido negocio de la experimentación animal y abracemos una tecnología ética, moderna, abierta y relevante a la fisiología humana. Sólo así evolucionaremos como comunidad científica y como sociedad.
BIBLIOGRAFÍA.
[1]European Dementia Monitor 2020. Comparing and benchmarking national dementia strategies and policies https://www.alzheimer-europe.org/sites/default/files/2021-11/European%20Dementia%20Monitor%202020%20%20Comparing%20and%20benchmarking%20national%20dementiastrategies%20and%20policies.pdf
[2]World Health Organization. Dementia https://www.who.int/news-room/fact-sheets/detail/dementia
[3]Li X, Feng X, Sun X, Hou N, Han F and Liu Y (2022) Global, regional, and national burden of Alzheimer’s disease and other dementias, 1990–2019. Front. Aging Neurosci. 14:937486. doi: https://doi.org/10.3389/fnagi.2022.937486
[4]Wimo A., Jönsson, J., and Gustavsson, A., 2009, Cost of illness and burden of dementia – the base option. Available at http://www.alzheimer-europe.org/Our-Research/European-Collaboration-on-Dementia/Cost-of-dementia/Cost-of-illness-and-burden-of-dementia
[5]Abidin M, Normal MRI Brain. Case study, Radiopaedia.org https://doi.org/10.53347/rID-153576
[6]Gaillard F, Alzheimer disease. Case study, Radiopaedia.org https://doi.org/10.53347/rID-22196
[7]Gaillard F, Lewy body dementia. Case study, Radiopaedia.org https://doi.org/10.53347/rID-28774
[8]Gaillard F, Vascular dementia. Case study, Radiopaedia.org https://doi.org/10.53347/rID-25641
[9]Lesit, M; Hartun, T (2019) «Inflammatory findings on species extrapolations: humans are definitely no 70-kg mice». https://pubmed.ncbi.nlm.nih.gov/23503654/
[10]AKHTAR A. The Flaws and Human Harms of Animal Experimentation. Cambridge Quarterly of Healthcare Ethics. 2015;24(4):407-419. doi:10.1017/S0963180115000079
[11]Cummings, J.L., Morstorf, T. & Zhong, K. Alzheimer’s disease drug-development pipeline: few candidates, frequent failures. Alz Res Therapy6, 37 (2014). https://doi.org/10.1186/alzrt269
[12] Taylor K, Gordon N, Langley G, Higgins W. Estimates for worldwide laboratory animal use in 2005. Altern Lab Anim. 2008 Jul;36(3):327-42. doi: 10.1177/026119290803600310. PMID: 18662096.
[13]Déclaration de Toulon. https://www.univ-tln.fr/Declaration-de-Toulon.html
[14]Gary W. Miller. The Exposome. A New Paradigm for the Environment and Health. Second edition. Academic Press, 2020.
[15] Killin LO, Starr JM, Shiue IJ, Russ TC. Environmental risk factors for dementia: a systematic review. BMC Geriatr. 2016 Oct 12;16(1):175. doi: 10.1186/s12877-016-0342-y. PMID: 27729011; PMCID: PMC5059894. https://doi.org/10.1186%2Fs12877-016-0342-y
[16] Killin, L.O.J., Starr, J.M., Shiue, I.J. et al. Environmental risk factors for dementia: a systematic review. BMC Geriatr 16, 175 (2016). https://doi.org/10.1186/s12877-016-0342-y
17]The Global Exposome Project, GNU Solidario https://www.gnusolidario.org/global-exposome/index.html
[18]Stiletto: A computational model of the cerebral perforating arteries in health and disease. https://www.gnusolidario.org/global-exposome/projects/stiletto/index.html
[19]Pantoni, L, Gorelik, P. Cerebral Small Vessel Disease. Cambridge Medicine, 2014
[20]Djulejić V, Marinković S, Milić V, Georgievski B, Rašić M, Aksić M, Puškaš L. Common features of the cerebral perforating arteries and their clinical significance. Acta Neurochir (Wien). 2015 May;157(5):743-54; discussion 754. doi: 10.1007/s00701-015-2378-8. Epub 2015 Mar 14. PMID: 25772345.
[21]Mencattini A, Mattei F, Schiavoni G, Gerardino A, Businaro L, Di Natale C and Martinelli E (2019) From Petri Dishes to Organ on Chip Platform: The Increasing Importance of Machine Learning and Image Analysis. Front. Pharmacol. 10:100. doi: 10.3389/fphar.2019.00100
[22]Ahn, Y.; An, J.-H.; Yang, H.-J.; Lee, D.G.; Kim, J.; Koh, H.; Park, Y.-H.; Song, B.-S.; Sim, B.-W.; Lee, H.J.; et al. Human Blood Vessel Organoids Penetrate Human Cerebral Organoids and Form a Vessel-Like System. Cells 2021, 10, 2036. https://doi.org/10.3390/cells10082036
[23] GNU Health, the Free/Libre digital health ecosystem . https://www.gnuhealth.org
[24] UniprotKB .- The UniProt Knowledgebase (https://www.uniprot.org)

 Vínculo humano animal y mordeduras caninas.
Vínculo humano animal y mordeduras caninas.